○ 현재, 유전자 진단시약(RT-PCR) 및 면역검사(항원검사, 항체검사) 등 코로나19 진단시약 제품이 임상적 성능시험을 거쳐 정식 허가를 신청하였고, 임상적 성능시험계획 승인을 받은 제품이 성능시험 중에 있습니다.
○ 코로나19 진단시약은 검체 내의 바이러스 유무를 확인하는 ‘유전자 진단시약(RT-PCR)’, ‘항원진단시약’과 검체 내의 바이러스에 대한 항체 유무를 확인하는 ‘항체진단시약’ 등 3종류가 있습니다.
| 구분 | 유전자 검사 |
항원 검사 | 항체 검사 |
| 검사 목적 | 코로나19 바이러스 유전자 유무 확인 |
코로나19 바이러스 특정 단백질 유무 확인 | 코로나19 바이러스에 대한 항체 생성여부 확인 |
| 검사 물질 | 바이러스 유전자 |
바이러스 특정 단백질 | 체내 생성 항체 |
| 사용 검체 | 코 또는 목의 점액, 가래(객담) |
코 또는 목의 점액 | 혈액 |
| 검사 시간 | 약 3 ~ 6시간 |
약 15분 | 약 15분 |
| 장점 | 정확도가 높아 확진용으로 사용 |
유전자 검사 대비 검사시간 짧고 비용 낮음 |
과거 감염이력 확인 가능, 검사시간 짧고 비용 낮음 |
| 단점 | 과거 감염 이력 확인 불가, 검사시간 길고 비용 높음 |
유전자 검사 대비 낮은 정확도, 확진용으로 사용 어려움 |
감염 초기 항체가 확인되지 않을 수 있고,검사당시 검체 내 바이러스 유무 직접 확인 어려움 |
| 측정 원리 | 바이러스 유전자를 증폭하여 감염여부 확인 |
바이러스와 결합한 특정 물질을 검출하여 바이러스 감염여부 확인 |
체내에 생성된 항체와 결합한 물질을 분석하여 항체 존재여부 확인 |
| 검사자 (사용자) |
의료인 또는 검사 전문가 |
의료인 또는 검사 전문가 | 의료인 또는 검사 전문가 |
○ ‘유전자 진단시약’은 환자 검체 내의 바이러스 유전자를 증폭하는 ‘분자진단(RT-PCR) 방식*’으로, 바이러스 유무를 확인하여 감염 여부를 진단합니다. 이 방식은 과학적으로 가장 정확도가 높아, 코로나19 확진용으로 사용하고 있습니다.
* 비인두 및 구인두 가검물 등 환자 검체에 포함된 미량의 바이러스 유전자를 분리하고 이를 증폭하여 바이러스 유무를 확인하는 방법
○ ‘항원 진단시약’은 바이러스의 특정 단백질을 인식하여 검체내의 바이러스 유무로 감염 여부를 확인합니다. 다만, 비인두‧구인두 등 검체를 그대로 사용하여 바이러스가 미량인 경우는 검사 결과에 영향을 줄 수 있습니다.
○ ‘항체 진단시약’은 바이러스 감염에 대한 면역반응으로 만들어진 항체의 생성 유무를 확인하는 제품으로, 항체가 생성되기 이전인 초기 감염단계에는 음성으로 진단될 수 있고 검사 당시의 검체 내 바이러스 유무를 직접적으로 확인하기에는 어려움이 있습니다.
번호 |
업체명 | 제품명 |
허가일 |
허가번호 |
비고 |
| 1 |
SD바이오센서(주) |
STANDARD™ M nCoV Real-Time Detection kit |
‘20.8.31. |
체외 제허 20-767호 | PCR |
| 2 |
(주)바이오세움 |
Real-Q 2019-nCoV Detection Kit |
‘20.10.6. |
체외 제허 20-860호 | PCR |
| 3 |
㈜시선바이오 머티리얼스 |
U-TOP™ COVID-19 Detection Kit Plus |
‘20.10.8. |
체외 제허 20-871호 | PCR |
| 4 |
(주)캔서롭 |
Q-Sens® COVID-19 Detection kit |
‘20.10.8. |
체외 제허 20-872호 | PCR |
| 5 |
(주)코젠바이오텍 |
PowerChek™ SARS-CoV-2, Influenza A&B Multiplex Real-time PCR Kit |
‘20.11.3. |
체외 제허 20-923호 | PCR |
| 6 |
SD바이오센서(주) |
STANDARD™ Q COVID-19 IgM/IgG Plus Test |
‘20.11.6. |
체외 제허 20-941호 | 항체 |
| 7 |
SD바이오센서(주) |
STANDARD™ Q COVID-19 Ag Test |
‘20.11.11. |
체외 제허 20-955호 | 항원 |
| 8 |
㈜시선바이오 머티리얼스 |
AQ-TOP™ COVID-19 Rapid Detection Kit Plus |
‘20.11.23. |
체외 제허 20-990호 | PCR |
| 9 |
(주)코젠바이오텍 |
PowerChek™ SARS-CoV-2 Real-time PCR Kit |
‘20.11.26. |
체외 제허 20-1000호 | PCR |
| 10 |
(주)씨젠 |
Allplex SARS-CoV-2 Assay |
‘20.12.7. |
체외 제허 20-1049호 | PCR |
| 11 |
(주)캔서롭 |
Q-Sens® COVID-19 Detection Kit V2 | ‘20.12.14. |
체외 제허 20-1088호 | PCR |
| 12 |
(주)수젠텍 |
SGTi-flex COVID-19 IgM/IgG |
‘20.12.18. |
체외 제허 20-1112호 | 항체 |
| 13 |
(주)젠바디 |
GenBody COVID-19 Ag |
‘20.12.24. |
체외 제허 20-1150호 | 항원 |
| 14 |
SD바이오센서(주) |
STANDARD™ F COVID-19 Ag FIA |
‘21.1.5. |
체외 제허 21-3호 | 항원 |
| 15 |
(주)바이오세움 |
Real-Q Direct SARS-CoV-2 Detection Kit |
‘21.1.20. |
체외 제허 21-50호 | PCR |
| 16 |
(주)씨젠 |
Allplex™ SARS-CoV-2/FluA/FluB/RSV Assay |
‘21.1.26. |
체외 제허 21-65호 | PCR |
| 17 |
에스디바이오센서(주) |
STANDARD™ F COVID-19 IgM/IgG Combo FIA |
‘21.1.26. |
체외 제허 21-66호 | 항체 |
| 18 |
(주)에스엠엘제니트리 |
Ezplex® SARS-CoV-2 Kit |
‘21.1.29. |
체외 제허 21-75호 | PCR |
| 19 |
바이오코아(주) 생명공학사업부 |
BioCore 2019-nCoV Real Time PCR Kit |
‘21.3.12. |
체외 제허 21-187호 | PCR |
| 20 |
(주)래피젠 |
BIOCREDIT COVID-19 Ag |
‘21.3.18. |
체외 제허 21-200호 | 항원 |
| 21 |
휴마시스(주) |
Humasis COVID-19 Ag Test |
‘21.3.18. |
체외 제허 21-201호 | 항원 |
| 22 |
(주)랩지노믹스 |
LabGunTM COVID-19 ExoFast RT-PCR Kit |
‘21.3.18. |
체외 제허 21-202호 | PCR |
| 23 |
(주)옵토레인 |
Dr. PCR™ Di20K COVID-19 Detection kit |
‘21.3.23. |
체외 제허 21-209호 | PCR |
| 24 |
㈜시선바이오 머티리얼스 |
U-TOP™ SARS-CoV-2 & Flu A/B |
‘21.4.1. |
체외 제허 21-244호 | PCR |
| 25 |
한국로슈진단(주) |
Elecsys Anti-SARS-CoV-2 |
‘21.4.16 |
체외 수허 21-100호 | 항체 |
| 26 |
지멘스헬시니어스(주) |
ADVIA Centaur SARS-CoV-2 Total (COV2T) |
‘21.4.16 |
체외 수허 21-101호 | 항체 |
| 27 |
(주)젠바디 |
GenBody COVID-19 IgM/IgG |
‘21.4.20 |
체외 제허 21-308호 | 항체 |
| 28 |
휴마시스(주) |
휴마시스 코비드-19 홈 테스트 |
‘21.4.23 |
체외 제허 21-321호 | 항원 (개인용) |
| 29 |
SD바이오센서(주) |
STANDARD™ Q COVID-19 Ag Home Test |
‘21.4.23 |
체외 제허 21-322호 | 항원 (개인용) |
| 30 |
(주)오상헬스케어 |
GeneFiner COVID-19 Fast RealAmp Kit |
‘21.4.26 |
체외 제허 21-329호 | PCR |
| 31 |
(주)바이오세움 |
Real-Q SARS-CoV-2/FluA/FluB Detection Kit |
‘21.4.26 |
체외 제허 21-330호 | PCR |
| 32 |
(주)바이오니아 |
AccuPower® RV1 Real-Time RT-PCR Kit (RV1-1111) |
‘21.4.30 |
체외 제허 21-339호 | PCR |
| 33 |
한국로슈진단(주) |
cobas SARS-CoV-2 & Influenza A/B |
‘21.5.4 |
체외 수허 21-115호 | PCR |
| 34 |
휴마시스(주) |
Humasis COVID-19 IgG/IgM Test |
‘21.5.6 |
체외 제허 21-352호 | 항체 |
| 35 |
에스지메디칼(주) |
R-FIND COVID-19 IgM ELISA |
‘21.5.6 |
체외 제허 21-357호 | 항체 |
| 36 |
에스지메디칼(주) |
R-FIND COVID-19 IgG ELISA |
‘21.5.6 |
체외 제허 21-359호 | 항체 |
| 37 |
에스지메디칼(주) |
R-FIND COVID-19 IgG/M/A ELISA |
‘21.5.6 |
체외 제허 21-360호 | 항체 |
| 38 |
(주)팍스젠바이오 |
PaxView® SARS-CoV-2 real-time RT-PCR Kit |
‘21.5.12 |
체외 제허 21-371호 | PCR |
| 39 |
(주)수젠텍 |
SGTi-flex COVID-19 Ag |
‘21.5.25 |
체외 제허 21-407호 | 항원 |
| 40 |
(주)바이오니아 |
AccuPower® RV1 Multiplex Kit (RV1-2112) |
‘21.5.26 |
체외 제허 21-413호 | PCR |
| 41 |
웰스바이오(주) |
careUS™ COVID-19 IgM/IgG Ab |
‘21.5.27 |
체외 제허 21-419호 | 항체 |
| 42 |
(주)엘지화학 |
AdvanSure™ SARS-CoV-2 IgG (S1) ELISA |
‘21.5.27 |
체외 제허 21-424호 | 항체 |
| 43 |
(주)지노믹트리 |
AccuraDTect™ COVID-19 RT-qPCR Kit |
‘21.6.17 |
체외 제허 21-487호 | PCR |
| 44 |
(주)에스엠엘제니트리 |
Ezplex® SARS-CoV2/RV Fast Kit |
‘21.6.21 |
체외 제허 21-494호 | PCR |
| 45 |
(주)젠바디 |
GenBody FIA COVID-19 Ag |
‘21.6.21 |
체외 제허 21-499호 | 항원 |
| 46 |
(주)에이엠에스바이오 |
A+CheQ COVID-19 RT-qPCR Detection kit |
‘21.6.22 |
체외 제허 21-506호 | PCR |
| 47 |
피씨엘(주) |
PCL COVID19 Ag Gold |
‘21.6.23 |
체외 제허 21-514호 | 항원 |
| 48 |
(주)진매트릭스 |
NeoPlex™ FluCOVID Kit |
‘21.7.1 |
체외 제허 21-543호 | PCR |
| 49 |
(주)래피젠 |
BIOCREDIT COVID-19 Ag Home Test Nasal |
‘21.7.13 |
체외 제허 21-595호 | 항원 (개인용) |
| 50 |
바디텍메드(주) |
ichroma™ COVID-19 Ag |
‘21.7.13 |
체외 제허 21-596호 | 항원 |
| 51 |
바디텍메드(주) |
AFIAS COVID-19 Ag |
‘21.7.15 |
체외 제허 21-608호 | 항원 |
| 52 |
솔젠트(주) |
DiaPlexQ™ Novel Coronavirus (2019-nCoV) Detection Kit |
‘21.7.22 |
체외 제허 21-626호 | PCR |
| 53 |
(주)녹십자엠에스 |
GENEDIA W COVID-19 Ag |
‘21.7.29 |
체외 제허 21-649 호 | 항원 |
| 54 |
프리시젼바이오(주) |
PBCheck COVID-19 Ag |
‘21.8.3 |
체외 제허 21-658 호 | 항원 |
| 55 |
(주)비비비 |
MARK-B™ COVID-19 Ag |
‘21.8.9 |
체외 제허 21-673 호 | 항원 |
| 56 |
프리시젼바이오(주) |
Exdia COVID-19 Ag |
‘21.8.10 |
체외 제허 21-674 호 | 항원 |
| 57 |
피씨엘(주) |
PCL SARS-CoV-2 IgG EIA |
‘21.8.12 |
체외 제허 21-688 호 | 항체 |
| 58 |
(주)미코바이오메드 |
COVID-19 Biokit IgG/IgM |
‘21.8.13 |
체외 제허 21-692 호 | 항체 |
| 59 |
(주)미코바이오메드 |
VERI-Q COVID-19 Ag Rapid Test |
‘21.8.20 |
체외 제허 21-702 호 | 항원 |
| 60 |
웰스바이오(주) |
careUS™ COVID-19 antigen |
‘21.8.25 |
체외 제허 21-718 호 | 항원 |
| 61 |
(주)진매트릭스 |
NeoPlex™ COVID-19 Detection |
‘21.8.27 |
체외 제허 21-729 호 | PCR |
| 62 |
아산제약(주)공도지점 |
Asan Easy Test COVID-19 Ag |
‘21.9.9 |
체외 제허 21-754 호 | 항원 |
| 63 |
(주)바이오니아 |
AccuPower® COVID-19 Multiplex Real-Time RT-PCR Kit (NCVM-1211) |
‘21.9.13 |
체외 제허 21-765 호 | PCR |
| 64 |
(주)한국애보트진단 |
Panbio™ COVID-19 Ag Rapid Test Device(Nasopharyngeal) |
‘21.9.28 |
체외 제허 21-799 호 | 항원 |
| 65 |
(주)미코바이오메드 |
Veri-Q COVID-19 Multiplex Detection Kit |
‘21.10.20 |
체외 제허 21-851 호 | PCR |
| 66 |
(주)케이에이치메디칼 |
RADI COVID-19 Detection Kit |
‘21.11.8 |
체외 제허 21-890 호 | PCR |
| 67 |
(주)원메디칼 |
WonMed Covid-19 Ag (WM COVAG-25T) |
‘21.11.10 |
체외 제허 21-895 호 | 항원 |
| 68 |
한국애보트(유) |
SARS-CoV-2 IgG II Quant Reagent Kit |
‘21.12.10 |
체외 수허 21-304 호 | 항체 |
| 69 |
㈜인트론바이오 테크놀로지 |
LiliF™ COVID-19 Multi Real-time RT-PCR Kit |
‘21.12.10 |
체외 제허 21-998 호 | PCR |
| 70 |
에스디바이오센서(주) |
STANDARD™ M10 SARS-CoV-2 |
‘21.12.21 |
체외 제허 21-1030 호 | PCR |
코로나19 항체검사시약이란?
○ 코로나19 바이러스(SARS-CoV-2) 항체가 혈액 내에 생성되었는지 확인하는데 도움을 주는 체외진단의료기기입니다.
○ 코로나19 항체검사시약의 용도는, 과거 감염 이력 확인, 항체 생성률 역학조사, 항체 반응 연구 등에 활용됩니다.
- 과거 코로나19 감염에 의한 항체 생성 여부만을 확인할 수 있어, 코로나19 감염 진단 목적으로 사용할 수 없습니다.
※(참고) 코로나19 감염 진단에는 바이러스 존재 여부를 확인하는 유전자 검사(PCR) 시약을 사용하며, 감염 진단의 보조적 수단으로 항원검사시약이 있습니다.
ㅇ 또한, 현재 항체검사시약은 코로나19에 대한 면역상태나 감염예방 능력 확인이나 백신 접종 후 항체 생성 여부를 확인할 수 없습니다.
코로나19 항체검사시약으로 면역력 확인 등이 부적절한 이유는?
○ 아직 코로나19 항체 생성 정도와 면역력 상관관계 등의 과학적 근거가 충분하지 않아 연구가 더 필요한 단계 임.
ㅇ 개인의 면역력이나 바이러스 전파 가능성 확인을 위한 항체검사는 적합하지 않습니다.
ㅇ 면역력은 항체에 의한 체액성 면역과 그 이외의 세포성 면역으로 평가되는 것으로 단순히 항체만으로 면역력을 평가할 수는 없습니다.
또한, 현재 식약처에서 허가된 항체검사시약은 코로나19 백신접종자를 대상으로 임상적 성능이 평가되지 않아, 코로나19에 대한 면역상태 또는 감염예방 능력 판단, 백신 접종 후 항체 생성 여부 확인에는 적합하지 않습니다.
코로나19 항체검사시약을 전문가용으로만 허가한 이유는?
○ 아직 코로나19 항체 생성 정도와 면역력 상관관계 등의 과학적 근거가 충분하지 않아 연구가 더 필요한 단계 임
- 항체검사시약에 대한 일반 소비자들의 사용목적·방법에 대한 오남용 우려와 이로 인한 방역체계 혼란을 방지하고자, 국내 방역여건과 해외의 도입 사례 등을 종합적으로 검토하고, 방역 당국 및 전문가 의견을 수렴하여 항체검사시약은 전문가용으로만 허가하기로 하였습니다.
코로나19 항체검사 결과의 의미는?
○ 항체검사 결과 ‘양성’은 과거 코로나19에 감염되었을 가능성을 의미하며, 양성 또는 음성 결과가 현재의 감염 여부나 백신 접종자를 포함한 개인의 면역상태 또는 감염예방 능력 여부를 나타내는 것은 아닙니다.
- 아직 항체의 생성시기, 장기간 유지 여부에 대해서는 과학적 근거가 충분하지 않아 연구가 더 필요한 단계이며,
- 혈액 채취 시기, 검사 시기 등의 여러 영향으로 검사 결과 위양성, 위음성 가능성이 있습니다.
- 따라서, 항체 검사 결과와 관계없이 방역수칙(마스크 착용, 거리두기 등) 및 백신 접종 안내사항을 반드시 준수하여야 합니다.
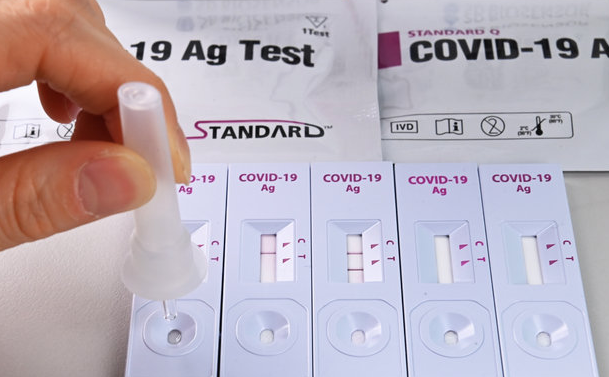
< 자가검사 키트의 올바른 사용방법 >
○ 식약처는 “자가검사키트는 코로나19 감염 진단이 아닌 보조 수단으로만 사용하고, 사용방법 및 주의사항 등을 준수하여 사용해달라”고 당부했습니다.
- 자가검사 키트는 의료인 또는 검사 전문가가 콧속 깊은 비인두에서 검체를 채취해 진행하는 유전자 검사(PCR) 방식에 비해 민감도가 낮은 단점이 있습니다.
- 코로나19 감염 의심 증상이 있거나 역학적 연관성이 있는 경우에는 자가검사 결과와 관계없이 즉시 선별 진료소 등을 방문해 반드시 유전자 검사(PCR)를 최우선으로 받아야 합니다.
- 따라서 자가검사키트 사용자는 제품의 허가 사항과 사용설명서를 충분히 숙지하고 정확하게 사용해야 하며, 검사 결과와 관계없이 마스크 착용·손 씻기 등 방역수칙을 철저하게 준수해야 합니다.
< 자가검사 키트의 허가·조건부 허가 절차와 현황 >
○ 자가검사 키트는 「체외진단의료기기법」과 「민원 처리에 관한 법률」 등에서 정한 요건과 심사기준에 따라 허가·심사가 진행됩니다.
- 식약처는 제품의 허가(변경 허가 포함)신청이 접수되면 「체외진단의료기기법」에 따라 제출자료를 검토합니다. 제출자료에 보완이 필요한 경우 「민원 처리에 관한 법률」에 따라 자료를 보완·제출토록 요청(최대 2회)하며, 최종 제출자료가 적합하면 허가하고 그렇지 않으면 신청 반려 처분합니다.




