식약처에서 발표된 2021년 건강기능식품 기능성원료 재평가 결과입니다.
기능성원료는 아래와 같습니다.
-엽록소 함유 식물
-스피루리나
-프로폴리스추출물
-감마리놀렌산 함유 유지(달맞이꽃)
-차전자피식이섬유
-폴리덱스트로스
-홍국
-홍국쌀
-콜레우스 포스콜리 추출물
[ 엽록소 함유 식물 ]

1. 원료명
○ 원료명 : 엽록소 함유 식물
2. 제조기준
○ 원재료 :
(가) 맥류약엽(보리, 밀, 귀리의 어린 싹) 또는 어린 잎
(나) 알팔파의 성숙한 잎, 줄기
(다) 엽록소를 함유한 식용해조류
(라) 맥류약엽, 알팔파, 식용해조류 이외의 식용식물
○ 기능성분(또는 지표성분) : 총엽록소를 맥류약엽은 2.4 mg/g 이상, 알팔파는 0.6
mg/g 이상, 식용해조류 및 기타식용식물은 1.2 mg/g 이상 함유하고 있어야 함
○ 제조 시 유의사항 : 없음
3. 제조방법
○ 상기 (가)∼(라)의 원재료의 경우에는 원재료를 그대로 또는 착즙 건조하여 제조
하여야 함
4. 기준 및 규격
가. 기능성분(또는 지표성분) 함량
○ 총 엽록소
(가) 원료성 제품 : 표시량 이상
(나) 최종제품 : 표시량의 80~120%
나. 중금속 및 미생물 규격
○ 대장균군 : 음성
다. 원료를 특정 지을 수 있는 성상, 물성 등
○ 성상 : 고유의 색택과 향미를 가지며 이미․이취가 없어야 함
5. 기능성
○ (기존) 기능성 내용 및 일일섭취량 : 피부건강 항산화에 도움을 줄 수 있음
총엽록소로서 8∼150 mg
○ 피부건강에 도움을 줄 수 있음
- 49-69세의 건강한 여성을 대상으로 엽록소 함유 식물 추출액을 90일 동안 섭취하
였을 때 주름이 유의적 감소하였고, 피부 탄력과 type I procollagen mRNA 발현이
유의적으로 증가하였음
○ 항산화에 도움을 줄 수 있음
- 인체적용시험에서 건강한 성인을 대상으로 밀싹 분말, 시금치를 섭취했을 때
MDA, TAS, SOD, DNA 손상 저해 등의 지표가 개선되어 항산화에 도움을 주는
것으로 나타남
6. 안전성
○ 49-69세의 여성을 대상으로 한 인체적용시험에서 엽록소 함유 식물을 섭취하였을
때, 이상증상이 관찰되지 않았음
7. 일일섭취량
○ (기존) 기능성 내용 및 일일섭취량 : 피부건강 항산화에 도움을 줄 수 있음
총 엽록소로서 8 ∼ 150 mg
○ (개선 제안) 현행유지
8. 섭취 시 주의사항
○ (기존) 없음
○ (개선 제안)
- 섭취하는 개인의 체질이나 건강특성에 따라 광 민감성, 알레르기 등의 이상증상
이 나타날 수 있으므로 섭취 후 이상사례 발생 시 섭취를 중단하고 전문가와 상
담할 것을 추가 제안함
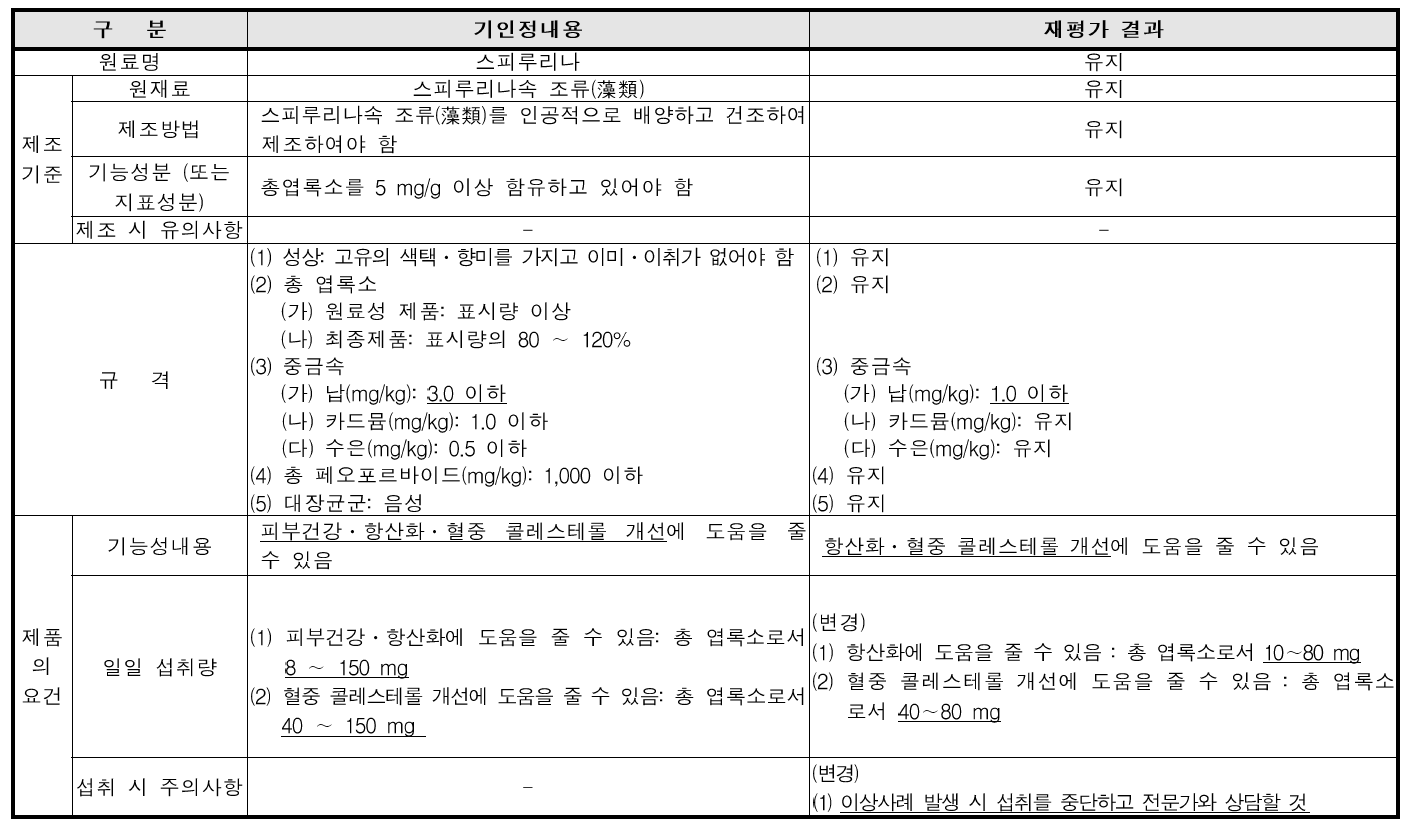
[ 스피루리나 ]
1. 원료명
○ 원료명 : 스피루리나
2. 제조기준
○ 원재료 : 스피루리나속 조류(藻類)
○ 기능성분(또는 지표성분) : 총엽록소를 5 mg/g 이상 함유하고 있어야 함
3. 제조방법
○ 스피루리나 속 조류(藻類)를 인공적으로 배양하고 건조하여 제조하여야 함
4. 기준 및 규격
가. 기능성분(또는 지표성분) 함량
○ 총 엽록소
- 원료성 제품 : 표시량 이상
- 최종제품 : 표시량의 80∼120%
나. 중금속 및 미생물 규격
○ 납(mg/kg) : 3.0 이하
○ 카드뮴(mg/kg) : 1.0 이하
○ 수은(mg/kg) : 0.5 이하
○ 총 페오포르바이드(mg/kg) : 1,000 이하
○ 대장균군 : 음성
※ (개선 제안) 다른 기능성 원료에 비해 납의 규격이 높은 것으로 판단되므로 영업자
관리기준으로 납 규격 재설정을 제안함
- 납(mg/kg) : 1.0 이하
다. 원료를 특정 지을 수 있는 성상, 물성 등
○ 고유의 색택과 향미를 가지며 이미·이취가 없어야 함
5. 기능성
○ (기존) 기능성 내용 : 피부건강·항산화·혈중 콜레스테롤 개선에 도움을 줄 수 있음
○ 피부건강에 도움을 줄 수 있음
- 스피루리나를 시험물질로 한 피부건강 관련 인체적용시험 자료가 없어 기능성
확인이 어려우므로, 피부건강 기능성 삭제
○ 항산화에 도움을 줄 수 있음
- 인체적용시험에서 성인, 60세 이상 노인, 고콜레스테롤 경계인, 환자를 대상으로 스
피루리나를 섭취했을 때 TBARS, TAS, SOD, MDA 등 항산화 관련 지표가 개선
되어 항산화에 도움을 주는 것으로 나타남
○ 혈중 콜레스테롤 개선에 도움을 줄 수 있음
- 성인, 60세 이상 노인, 고콜레스테롤 경계인, 환자를 대상으로 스피루리나를 섭취하
였을 때 혈중 총 콜레스테롤, LDL 및 HDL 콜레스테롤 등의 지표가 유의적으로 개
선되어 혈중 콜레스테롤 개선에 도움을 주는 것으로 나타남
6. 안전성
○ 동물시험에서 설치류(rat, mouse)에게 스피루리나를 경구 투여 하였을 이상증상 및
독성이 관찰되지 않았음
○ 인체적용시험에서 간 기능지표의 유의적 변화, 중대한 이상증상이 관찰되지 않았음
○ 스피루리나 섭취에 따른 이상사례는 주로 메스꺼움, 설사, 구토, 피로, 두통, 현기증,
가려움증, 발진 및 복부 경련으로 보고되고 있음
7. 일일섭취량
○ (기존) 일일섭취량
① 피부건강·항산화에 도움을 줄 수 있음 : 총 엽록소로서 8∼150 mg
② 혈중 콜레스테롤 개선에 도움을 줄 수 있음 : 총 엽록소로서 40∼150 mg
○ (개선 제안)
① 항산화에 도움을 줄 수 있음 : 총 엽록소로서 10∼80 mg
② 혈중 콜레스테롤 개선에 도움을 줄 수 있음 : 총 엽록소로서 40∼80 mg
8. 섭취 시 주의사항
○ (기존) 섭취 시 주의사항 : 없음
○ (개선 제안)
- 섭취하는 개인의 체질이나 건강특성에 따라 광 민감성 등이 나타날 수 있으므로
섭취 후 이상사례 발생 시 섭취를 중단하고 전문가와 상담할 것을 추가 제안함
[프로폴리스 추출물]

1. 원료명
○ 원료명 : 프로폴리스추출물
2. 제조기준
○ 원재료 : 꿀벌이 식물에서 채취한 수지에 자신의 분비물을 혼합하여 만든 프로폴리스
○ 기능성분(또는 지표성분)의 함량 : 총 플라보노이드를 10 mg/g이상 함유하고 있어야
하며, 파라(ρ)-쿠마르산 및 계피산이 확인되어야 함
3. 제조방법
○ 제조방법 : 상기의 원재료에서 왁스를 제거하고 물, 주정(물 주정 혼합물 포함) 또는
이산화탄소(초임계추출)로 추출하여 제조하여야 함
○ 제조 시 유의사항 : 디에틸렌글리콜을 사용하여서는 아니 됨
4. 기준 및 규격
가. 기능성분(또는 지표성분)의 함량
○ 총 플라보노이드를 10 mg/g이상 함유하고 있어야 하며, 파라(ρ)-쿠마르산 및 계피산이
확인되어야 함
나. 중금속 및 미생물 규격
○ 납(mg/kg) : 5.0 이하
○ 디에틸렌글리콜 : 불검출
○ 테트라싸이클린(mg/kg) : 불검출
○ 클로르테트라싸이클린(mg/kg) : 불검출
○ 대장균군 : 음성
※ (개선 제안) 기능성 원료에 비해 납의 규격이 높은 것으로 판단되므로 영업자 관리
기준으로 납 규격 재설정을 제안함
- 납(mg/kg) : 1.0 이하
다. 원료를 특정 지을 수 있는 성상, 물성 등
○ 성상 : 고유의 색택과 향미를 가지며 이미․이취가 없어야 함
5. 기능성
○ (기존) 기능성 내용 및 일일섭취량
- 항산화에 도움을 줄 수 있음 : 총 플라보노이드로서 16∼17 mg
- 구강에서의 항균작용에 도움을 줄 수 있음 : 구강에 직접 접촉할 수 있는 형태에 한
하며, 섭취량을 적용하지 않음
○ 항산화에 도움을 줄 수 있음
- 인체적용시험에서 건강한 성인 및 흡연자 등을 대상으로 프로폴리스 추출물을 섭
취하였을 때 GSH, TAC, TBARS, SOD, MDA 등 항산화 관련 지표가 개선되어
항산화에 도움을 줄 수 있는 것으로 나타남
○ 구강에서 항균작용에 도움을 줄 수 있음
- 인체적용시험에서 유아, 구강 관련 환자를 대상으로 구강에 프로폴리스 추출물을
접촉시켰을 때 구강의 S. mutans, 구강염, 통증, 치주관련지표 등에서 유의적으로
개선되어 구강에서 항균작용에 도움을 줄 수 있는 것으로 나타남
6. 안전성
○ 인체적용시험에서 건강한 성인 및 질병보유자에게 프로폴리스 추출물을 섭취하도록
하였을 때, 관련된 이상 증상은 보고되지 않았음
○ NIHN과 Health Canada에 따르면 프로폴리스 섭취로, 위장, 호흡기, 피부 등의
알레르기 반응으로 인한 염증, 과민반응이 발생할 수 있으며, 국내·외 이상사례에서
프로폴리스 추출물 섭취 후, 알레르기 관련 증상이 발생한 사례가 확인되었음
7. 일일섭취량
○ (기존) 일일섭취량 : 총 플라보노이드로서 16∼17 mg
○ (개선 제안) : 항산화 기능성 관련한 인체적용시험에서 안전성과 기능성이 나타난 일일섭취량으로 변경 제안[51, 58]
- 항산화에 도움을 줄 수 있음 : 총 플라보노이드로서 20∼40 mg
- 구강에서의 항균작용에 도움을 줄 수 있음 : 현행유지
8. 섭취 시 주의사항
○ (기존) 섭취 시 주의사항 : 프로폴리스에 알레르기를 나타내는 사람은 섭취에 주의
○ (개선 제안)
- 섭취하는 개인의 체질이나 건강특성에 따라 섭취 후 호흡기, 피부 등의 알레르기
반응과 같은 이상증상이 발생할 수 있으므로, 섭취 후 이상사례 발생 시 섭취를 중단
하고 전문가와 상담할 것을 추가 제안함
[ 감마리놀렌산 함유 유지 ]

1. 원료명
○ 원료명 : 감마리놀렌산 함유 유지
2. 제조기준
○ 원재료 : 감마리놀렌산 함유 유지
- 달맞이 꽃(Evening primrose, Oenothera biennis, Oenothera caespitesa, Oenothera
hookeri, Oenothera odorata) 종자, 보라지(Borage, Borago officinalis L.) 종자, 까막까
치밥(Black currant, Ribes grossulalis, Ribes ussuriense, Ribes nigrum) 종자
○ 기능성분(또는 지표성분) : 감마리놀렌산
○ 제조 시 유의사항 : 없음
3. 제조방법
○ 원재료를 압착, 헥산 또는 이산화탄소(초임계추출)를 이용하여 유지를 추출한 후
여과하여 제조하여야 함
4. 기준 및 규격
가. 기능성분(또는 지표성분) 함량
○ 감마리놀렌산이 70 mg/g 이상이어야 함
나. 중금속 및 잔류용매 규격
○ 잔류용매(mg/kg) : 5.0 이하(헥산을 사용한 경우)
○ 대장균군 : 음성
다. 원료를 특정 지을 수 있는 성상, 물성 등
○ 성상: 고유의 색택과 향미를 가지며 이미 이취가 없어야 함
5. 기능성
○ (기존) 기능성 내용 및 일일섭취량
- 혈중 콜레스테롤 개선 혈행개선에 도움을 줄 수 있음 : 감마리놀렌산으로서 240
∼ 300 mg
- 월경전 변화에 의한 불편한 상태 개선에 도움을 줄 수 있음 : 감마리놀렌산으로서
210∼ 300 mg
- 면역과민반응에 의한 피부상태 개선에 도움을 줄 수 있음 : 감마리놀렌산으로서
160∼ 300 mg
○ 혈중 콜레스테롤 개선에 도움을 줄 수 있음
- 인체적용시험에서 건강한 성인, 고지혈증 환자, 노인을 대상으로 감마리놀렌산 함
유 유지를 섭취하였을 때 총 콜레스테롤, HDL, LDL, triglyceride 등이 유의적으로
개선되어 혈중 콜레스테롤 개선에 도움을 줄 수 있는 것으로 나타남
○ 혈행개선에 도움을 줄 수 있음
- 인체적용시험에서 건강한 성인, 고지혈증 환자, 노인을 대상으로 감마리놀렌산 함
유 유지를 섭취하였을 때 혈액응고(ThromboxaneB2, MDA, 혈소판 응집 등) 및 혈
압관련 지표(노르에피네프린)가 유의적으로 개선되어 혈중 콜레스테롤 개선에 도
움을 줄 수 있는 것으로 확인됨
○ 월경전 변화에 의한 불편한 상태 개선에 도움을 줄 수 있음
- 인체적용시험에서 PMS 증상을 앓고 있는 여성을 대상으로 감마리놀렌산 함유 유
지를 섭취하였을 때 PMS 증상 관련 지표(PMS score, PRISM score) 및 그 세부항
목에서 유의적으로 개선되어 월경전 변화에 의한 불현한 상태 개선에 도움을 주는
것으로 확인됨
○ 면역과민반응에 의한 피부상태 개선에 도움을 줄 수 있음
- 인체적용시험에서 아토피성 피부염을 앓고 있는 어린이 및 성인을 대상으로 감마
리놀렌산 함유 유지를 섭취하였을 때 아토피 관련 설문(SCORAD INDEX, EASI)
및 그 세부항목, 경피수분손실량 등에서 유의하게 개선된 것으로 나타나 면역과민
반응에 의한 피부상태 개선에 도움을 줄 수 있을 것으로 판단됨
6. 안전성
○ 초파리를 대상으로 한 유전독성시험에서 125 μl/ml 이하의 농도에서는 생존률에 대
한 유의적 차이가 없었으며, 유전적인 돌연변이능도 관찰되지 않았음
○ 인체적용시험에서 건강한 성인남녀, 아토피 증상을 가진 성인 및 어린이, PMS 증
상을 가진 여성을 대상으로 감마리놀렌산 함유 유지를 섭취하였을 때 심각한 이상
증사례는 확인된 바 없으며, 안전성에 문제가 없었음
○ 미국의 CAERS 및 캐나다의 이상사례 데이터베이스에 따르면 감마리놀렌산
함유 유지 섭취 후 위장장애, 발진, 고혈압, 현기증, 낭포성 여드름 등의 이상증상이
발생할 수 있음
7. 일일섭취량
○ (기존)
- 혈중 콜레스테롤 개선 혈행개선에 도움을 줄 수 있음 : 감마리놀렌산으로서 240
∼ 300 mg
- 월경전 변화에 의한 불편한 상태 개선에 도움을 줄 수 있음 : 감마리놀렌산으로서
210∼ 300 mg
- 면역과민반응에 의한 피부상태 개선에 도움을 줄 수 있음 : 감마리놀렌산으로서
160∼ 300 mg
○ (개선 제안)
- 현행유지
8. 섭취 시 주의사항
○ (기존) 섭취 시 주의사항 : 영 유아 어린이는 섭취 전 의사와 상담한 후 섭취할
것(면역과민반응에 의한 피부상태 개선에 도움을 줄 수 있다는 기능성을 표시 판
매하는 경우에 한함)
○ (개선 제안) 다음과 같이 섭취 시 주의사항 신설을 제안함
- 영 유아 어린이는 섭취 전 전문가와 상담할 것(면역과민반응에 의한 피부상태
개선에 도움을 줄 수 있다는 기능성을 표시 판매하는 경우에 한함) (기존)
○ 섭취하는 개인의 체질이나 건강특성에 따라 감마리놀렌산 함유 유지 섭취 후 위장
장애, 두통, 현기증 등의 이상증상이 발생할 수 있으므로 이상사례 발생 시 섭취를
중단하고 전문가와 상담할 것을 추가 제안함
[ 차전자피식이섬유 ]

1. 원료명
○ 원료명 : 차전자피식이섬유
2. 제조기준
○ 원재료 : 차전자피(Plantago ovata 또는 Plantago spp.)껍질
○ 기능성분(또는 지표성분) : 식이섬유를 790 mg/g이상 함유하고 있어야 함
3. 제조방법
○ 원재료를 그대로 분쇄하여 제조하여야 함
4. 기준 및 규격
가. 기능성분(또는 지표성분) 함량
○ 식이섬유를 790 mg/g이상 함유하고 있어야 함
- 원료성 제품 : 표시량 이상, 최종제품 : 표시량의 80% 이상
나. 중금속 및 미생물 규격
○ 대장균군 : 음성
다. 원료를 특정 지을 수 있는 성상, 물성 등
○ 성상 : 고유의 색택·향미를 가지고 이미·이취가 없어야 함
5. 기능성
○ (기존) 기능성 내용 : 혈중 콜레스테롤 개선·배변활동 원활에 도움을 줄 수 있음
○ 혈중 콜레스테롤 개선에 도움을 줄 수 있음
- 인체적용시험에서 고지혈증 환자, 건강한 청소년, 당뇨환자를 대상으로 차전자피를
섭취했을 때 총 혈청 콜레스테롤, LDL 콜레스테롤, HDL 콜레스테롤 등의 콜레스테롤
관련 지표가 유의적으로 개전되어 혈중 콜레스테롤 개선에 도움을 주는 것으로
나타남
○ 배변활동 원활에 도움을 줄 수 있음
- 인체적용시험에서 만성 변비환자, 당뇨 환자를 대상으로 차전자피를 섭취했을 때
배변빈도, 배변무게, 변비증상 등이 유의적으로 개선되는 것으로 나타남
6. 안전성
○ 독성시험에서 쥐(rat)에게 차전자피 혼합물을 경구 투여하였을 때, 이상증상은 관찰
되지 않았음
○ 인체적용시험에서 건강한 청소년, 변비환자, 당뇨환자 대상으로 차전자피를 섭취했을 때
혈청학적 결과, 생화학 결과에서 유의적 변화가 나타나지 않았으며 이상증상은 보고
되지 않았음
○ Health Canada, EMA에 따르면 차전자피 섭취로 복통, 구토, 호흡문제, 알레르기
등의 증상이 발생할 수 있으며, 즉시 전문가 상담할 것을 권고하고 있음
7. 일일섭취량
○ (기존) 일일섭취량 :
- 혈중 콜레스테롤 개선에 도움을 줄 수 있음 : 차전자피 식이섬유로서 5.5 g 이상
- 배변활동 원활에 도움을 줄 수 있음 : 차전자피 식이섬유로서 3.9 g 이상
○ (개선 제안) 혈중 콜레스테롤 개선· 배변활동 원활과 관련한 인체적용시험에서 안
전성과 기능성이 나타난 일일섭취량으로 변경 제안
- 혈중 콜레스테롤 개선에 도움을 줄 수 있음 : 차전자피 식이섬유로서 6.0 g 이상
- 배변활동 원활에 도움을 줄 수 있음 : 차전자피 식이섬유로서 5.0 g 이상
8. 섭취 시 주의사항
○ (기존) 섭취 시 주의사항
- 반드시 충분한 물과 함께 섭취할 것(액상제외)
○ (개선 제안)
- 섭취하는 개인의 체질이나 건강 특성에 따라 복통, 구토, 호흡문제, 알레르기 등의
이상사례 발생 시 섭취를 중단하고 전문가와 상담할 필요가 있음을 추가할 것을
제안함
[ 폴리덱스트로스 ]

1. 원료명
○ 원료명 : 폴리덱스트로스
2. 제조기준
○ 원재료 : 구연산과 같은 유기산을 사용하여 글루코스와 솔비톨로부터 합성하여 평
균 중합도(단당의 결합수)가 12 정도가 되도록 제조하여야 함
○ 기능성분(또는 지표성분) : 식이섬유를 650 mg/g 이상 함유하고 있어야 함
3. 제조방법
○ 구연산과 같은 유기산을 사용하여 글루코스와 솔비톨로부터 합성하여 평균 중합도
(단당의 결합수)가 12 정도가 되도록 제조하여야 함
4. 기준 및 규격
가. 기능성분(또는 지표성분) 함량
○ 식이섬유를 650 mg/g 이상 함유하고 있어야 함
- 원료성 제품 : 표시량 이상, 최종제품 : 표시량의 80% 이상
나. 중금속 및 미생물 규격
○ 중금속 : 납(mg/kg) 0.5 이하
○ 대장균군 : 음성
다. 원료를 특정 지을 수 있는 성상, 물성 등
○ 성상 : 고유의 색택·향미를 가지고 이미·이취가 없어야 함
5. 기능성
○ (기존) 기능성 내용 : 배변활동 원활에 도움을 줄 수 있음
○ (기존) 일일섭취량 : 폴리덱스트로스 식이섬유로서 4.5 ∼ 12 g
○ 배변활동 원활에 도움을 줄 수 있음
- 인체적용시험에서 건강한 성인, 혈액투석 환자, 변비환자를 대상으로 폴리덱스트로
스를 섭취하도록 했을 때 배변횟수, 배변량, 배변의 운동성 등은 유의적으로 증가
하였고, 대변의 pH는 유의적으로 감소하여 배변활동 원활 관련 지표가 개선되는
것으로 나타났음
○ (개선 제안) 현행유지
6. 안전성
○ 독성시험에서 돼지, 쥐(rat)에게 폴리덱스트로스를 투여 했을 때, 혈액학적 지표, 장
기의 변화 및 이상증상이 관찰되지 않았음
○ 건강한 성인과 어린이, 변비가 있는 어린이를 대상으로 한 인체적용 시험에서 폴리
덱스트로스를 섭취하였을 때, 이상증상은 나타나지 않았음
7. 일일섭취량
○ (기존) 일일섭취량 : 배변활동 원활에 도움을 줄수 있는 기능성 연구보고서에 따라
폴리덱스트로스 식이섬유로서 4.5 ∼ 12 g
○ (개선 제안) 현행 유지
8. 섭취 시 주의사항
○ (기존) 섭취 시 주의사항
- 반드시 충분한 물과 함께 섭취할 것(액상제외)
○ (개선 제안)
- 섭취하는 개인의 체질이나 건강특성에 따라 설사, 위경련 등의 이상증상이 나타날
수 있으므로, 섭취 후 이상사례 발생 시 섭취를 중단하고 전문가와 상담할 것을
추가 제안함
[ 홍 국 ]

1. 원료명
○ 원료명 : 홍국
2. 제조기준
○ 원재료 : 쌀, 홍국균(Monascus anka, Monascus purpures, Monascus pilosus,
Monascus ruber )
○ 기능성분(또는 지표성분)의 함량 : 총 모나콜린 K를 0.5 mg/g 이상 함유하고 있어야
하며, 활성형 모나콜린 K가 확인되어야 함
○ 제조 시 유의사항 : 없음
3. 제조방법
○ 쌀(찐쌀을 제외)에 홍국균을 접종하여 고체발효시킨 후 분말화하여 제조하여야 함
4. 기준 및 규격
가. 기능성분(또는 지표성분) 함량
○ 총 모나콜린 K
(가) 원료성 제품 : 표시량 이상
(나) 최종제품 : 표시량의 80∼120%
○ 활성형 모나콜린 K : 확인
○ 시트리닌(mg/kg) : 0.05 이하
○ 대장균군 : 음성
5. 기능성
○ 혈중 콜레스테롤 개선에 도움을 줄 수 있음
- 인체적용시험에서 건강한 성인, 고콜레스테롤증 환자, 심근경색 환자를 대상으로
홍국을 섭취하였을 때, 총 콜레스테롤, HDL, LDL, Triglyceride 등이 유의적으로 개선 되어 혈중 콜레스테롤 개선에 도움을 줄 수 있는 것으로 확인됨
○ (개선 제안) 현행유지
6. 안전성
○ 쥐(rat)를 대상으로 홍국을 투여한 단회 및 반복투여 독성시험에서 독성학정 이상
반응은 관찰되지 않았음
○ 인체적용시험에서 건강한 성인남녀, 이상지질혈증 환자 및 관상동맥질환자 대상으로
홍국 분말을 섭취하였을 때 혈액검사, 간 및 신장기능 검사 결과 유의적인 변화는 없었
으며 중대한 이상 증상이 관찰되지 않았음
○ 홍국의 기능성분인 모나콜린 K는 고지혈증 치료제인 로바스타틴과 동일한 물질로
알려져 있으며 이상증상도 이와 유사하게 간 질환 및 근육·골격 손상 등이 나타남
○ NICCH, ANSES, NIHN에서 임산부, 수유부 및 어린이를 대상으로 섭취를 피하도록
권고하고 있으며, 간 질환이 있는 경우 섭취를 피할 것이라는 주의사항이 있음
○ 홍국에 포함될 수 있는 시트리닌은 독성물질로 발효에 의해 형성될 수 있으며, 유럽
연합 집행위원회(EU Commission)에서는 쌀 기반 식품의 최대 허용 시트리닌 함량을
2,000μg/kg에서 100 μg/kg으로 낮췄으며(2020년 4월 1일부터 적용), 국내에서는 50
μg/kg 이하로 관리하고 있음
7. 일일섭취량
○ 총 모나콜린 K로서 4∼8 mg
○ (개선 제안) 현행유지
8. 섭취 시 주의사항
○ (기존) 섭취 시 주의사항 : 없음
○ (개선 제안) 다음과 같이 섭취 시 주의사항 신설을 제안함
- NICCH, ANSES, NIHN에서 어린이, 임산부 및 수유부 등 취약계층이 홍
국을 섭취하는 것은 위험할 수 있으므로 섭취를 피하도록 권고하고 있으므로 어린
이, 임산부 및 수유부의 홍국 섭취에 대한 주의사항 설정을 추가 제안함
- ANSES, NIHN에서 간 질환이 있는 사람의 섭취를 피할 것을 권고하고 있고,
홍국의 기능성분인 모나콜린 K는 고지혈증 치료제인 로바스타틴과 동일한 물질로
알려져 있으며 홍국과 스타틴을 동시에 섭취할 경우 과다 복용 및 부작용 발
생할 수 있으므로 간 질환이 있거나, 고지혈증 치료제 복용 시 홍국 섭취를 피할
것을 추가 제안함
- 섭취하는 개인의 체질이나 건강특성에 따라 섭취 후 근골격계 이상증상, 위장장애 등과
같은 이상증상이 발생할 수 있으므로, 섭취 후 이상사례 발생 시 섭취를 중단하고 전
문가와 상담할 필요가 있음
[ 홍국쌀 ]

1. 원료명
○ 원료명 : 홍국쌀
2. 제조기준
○ 원재료 : 쌀, 홍국균
○ 기능성분(또는 지표성분)의 함량 : 총 모나콜린 K를 0.5 mg/g 이상 함유하고 있어
야 하며, 활성형 모나콜린 K가 확인되어야 함
○ 제조 시 유의사항 : 시트리닌이 0.05 mg/kg 이하이어야 함
3. 제조방법
○ 쌀세척 → 1차 멸균 → 냉각 → 홍국균 접종 → 순수배양 → 2차 멸균 → 건조 →
포장
* 홍국쌀은 건강기능식품 원료 ‘홍국’을 제조하는 방법과 동일하나 분쇄 단계를 거치
지 않은 것이 다른 점이며, 쌀의 형태로 섭취하는 원료임
4. 기준 및 규격
가. 기능성분(또는 지표성분) 함량
○ 총 모나콜린 K
(가) 원료 : 표시량 이상
(나) 최종제품 : 표시량의 80∼120%
나. 시트리닌(mg/kg) : 0.05 이하
다. 원료의 미생물 규격
○ 대장균군 : 음성
라. 최종제품의 기타 규격
○ 식품위생법 제7조제1항에서 정하는 「식품등의 기준 및 규격」에 적합하여야 함
○ 영양소 함량 기준
- 총지방 10 g 이하, 포화지방 3 g 이하, 당 15 g 이하, 나트륨 400 mg 이하
5. 기능성
○ 혈중 콜레스테롤 개선에 도움을 줄 수 있음
- 인체적용시험에서 건강한 성인, 고콜레스테롤증 환자, 심근경색 환자를 대상으로
홍국을 섭취하였을 때, 총 콜레스테롤, HDL 콜레스테롤, LDL 콜레스테롤,
Triglyceride 등이 유의적으로 개선되어 혈중 콜레스테롤 개선에 도움을 줄 수 있
는 것으로 확인됨
○ (개선 제안) 현행유지
6. 안전성
○ 쥐(rat)를 대상으로 홍국을 투여한 단회 및 반복투여 독성시험에서 독성학정 이상
반응은 관찰되지 않았음
○ 인체적용시험에서 건강한 성인남녀, 이상지질혈증 환자 및 관상동맥질환자 대상으로
홍국 분말을 섭취하였을 때 혈액검사, 간 및 신장기능 검사 결과 유의적인 변화는 없었
으며 중대한 이상 증상이 관찰되지 않았음
○ 홍국의 기능성분인 모나콜린 K는 고지혈증 치료제인 로바스타틴과 동일한 물질로
알려져 있으며 이상증상도 이와 유사하게 간 질환 및 근육·골격 손상 등이 나타남
○ NICCH, ANSES, NIHN에서 임산부, 수유부 및 어린이를 대상으로 섭취를 피하도록
권고하고 있으며, 간 질환이 있는 경우 섭취를 피할 것 이라는 주의사항이 있음
○ 홍국에 포함될 수 있는 시트리닌은 독성 물질로 발효에 의해 형성될 수 있으며,
유럽연합 집행위원회(EU Commission)에서는 쌀 기반 식품의 최대 허용 시트리닌
함량을 2,000μg/kg에서 100 μg/kg으로 낮췄으며(2020년 4월 1일부터 적용), 국내
에서는 50 μg/kg 이하로 관리하고 있음
7. 일일섭취량
○ 총 모나콜린 K로서 4∼8 mg
8. 섭취 시 주의사항
○ (기존) 섭취 시 주의사항 : (건강기능식품공전) 해당사항 없음
○ (개선 제안) 다음과 같이 섭취 시 주의사항 신설을 제안함
- NICCH, ANSES, NIHN에서 어린이, 임산부 및 수유부 등 취약계층이
홍국을 섭취하는 것은 위험할 수 있음으로 섭취를 피하도록 권고하고 있으므로 어린
이, 임산부 및 수유부의 홍국 섭취에 대한 주의사항 설정을 추가 제안함
- ANSES, NIHN에서 간 질환이 있는 사람의 섭취를 피할 것을 권고하고 있고,
홍국의 기능성분인 모나콜린 K는 고지혈증 치료제인 로바스타틴과 동일한 물질로
알려져 있으며 홍국과 스타틴을 동시에 섭취할 경우 과다 복용 및 부작용 발
생할 수 있으므로 간 질환이 있거나, 고지혈증 치료제 복용 시 홍국 섭취를 피할
것을 추가 제안함
- 섭취하는 개인의 체질이나 건강특성에 따라 섭취 후 근골격계 이상증상 등과 같은
이상증상이 발생할 수 있으므로, 섭취 후 이상사례 발생 시 섭취를 중단하고 전
문가와 상담할 필요가 있음
[ 콜레우스 포스콜리 추출물 ]

1. 원료명
○ 원료명 : 콜레우스 포스콜리 추출물, 콜레우스 포스콜리 추출물 Forslean
* 콜레우스 포스콜리 추출물 2개 원료 원료명 동일
2. 제조기준
○ 원재료
- 건강기능식품 기능성원료 인정서(제 2009-47호, 제 2011-42호, 제 2012-5호)를 따름
○ 제조방법
- 건강기능식품 기능성원료 인정서(제 2009-47호, 제 2011-42호, 제 2012-5호)를 따름
○ 기능성분(또는 지표성분)
- 건강기능식품 기능성원료 인정서(제 2009-47호, 제 2011-42호, 제 2012-5호)를 따름
○ 제조 시 유의사항 : 없음
3. 제조방법 : 업체별 제조방법에 따름(기능성원료 인정서)
- 건강기능식품 기능성원료 인정서(제 2009-47호, 제 2011-42호, 제 2012-5호)를 따름
4. 기준 및 규격
가. 기능성분(또는 지표성분) 함량
- 건강기능식품 기능성원료 인정서(제 2009-47호, 제 2011-42호, 제 2012-5호)를 따름
나. 중금속 규격

※ (개선 제안) 일부 원료의 중금속 규격이 다른 원료에 비해 높은 것으로 판단되어
다음과 같이 중금속 규격 재설정을 제안함
(1) 납(mg/kg) : 1.0 이하
(2) 총비소(mg/kg) : 1.0 이하
(3) 카드뮴(mg/kg) : 0.5 이하
(4) 총수은(mg/kg) : 0.5 이하
다. 미생물 규격
- 건강기능식품 기능성원료 인정서(제 2009-47호, 제 2011-42호, 제 2012-5호)를 따름
5. 기능성
○ (기존) 기능성 내용 및 일일섭취량 : 체지방 감소에 도움을 줄 수 있음, 콜레우스 포
스콜리 추출물로서 500 mg/일
○ 인체적용시험에서 과체중의 성인 또는 건강한 성인을 대상으로 콜레우스 포스콜리
추출물을 6∼12주간 섭취했을 때, 체중, 체지방, BMI 등은 유의적으로 감소하였고, 제지방은 유의적으로 증가하여 체지방 감소에 도움을 주는 것으로 확인됨
○ (개선 제안) 현행유지
6. 안전성
○ 설치류(rat, mice)를 대상으로 한 단회 및 반복투여 독성시험에서 이상중상 및 독성이
관찰되지 않았으며, 유전독성 실험에서도 독성은 나타나지 않았고,
간독성 관련한 보고가 있었으나 이를 뒷받침할 만한 근거가 부족함
○ 인체적용시험에서 과체중의 성인 또는 건강한 성인을 대상으로 콜레우스 포스콜리
추출물을 섭취했을 때 혈액학적 지표의 이상변화는 관찰되지 않았으며, 이상증상도
보고되지 않았음
○ 저혈압 환자나 혈압약을 복용 중인 사람은 섭취를 자제해야 하며, 콜레우스 포
스콜리의 지표성분인 포스콜린은 항응고제 및 혈소판 응집제와 동시에 사용 시
출혈의 위험이 있을 수 있음
○ 어린이, 수유 중인 여성, 임산부의 경우 안전성에 대한 연구가 충분히 진행되지 않
았기 때문에 주의해서 섭취해야함
○ 과복용시 복통, 두통, 홍조, 소화불량, 위산 증가 등의 증상이 발생할 수 있으며,
콜레우스포스 섭취로 인한 가장 빈번한 이상증상은 소화기계 증상으로 이중 대부
분이 설사 증상으로 나타났음
7. 일일섭취량
○ (기존) 콜레우스 포스콜리 추출물로서 500 mg
○ (개선제안) 현행유지
8. 섭취 시 주의사항
○ (기존) 섭취 시 주의사항(업체 제출자료)
① 항응고제 또는 혈압조절제를 복용하시거나 혈압이 낮으신 분은 섭취에 주의
② 임산부, 수유여성, 어린이는 섭취에 주의
○ (개선 제안)
- 섭취하는 개인의 체질이나 건강특성에 따라 설사 등의 이상증상이 나타날 수 있으
므로 이상사례 발생 시 섭취를 중단하고 전문가와 상담할 것을 추가 제안함
겨울철 노로바이러스 식중독
Q1. 노로바이러스가 무엇이며 증상이 어떠한가요? ❍ 노로바이러스는 오염된 음식물이나 물 등을 통해 섭취할 경우 사람에게 식중독을 일으키는 장관계 바이러스의 일종입니다. ❍ 바이러스에
daily-standup.tistory.com
코로나 검사 시간 및 검사키트 허가 기업
○ 현재, 유전자 진단시약(RT-PCR) 및 면역검사(항원검사, 항체검사) 등 코로나19 진단시약 제품이 임상적 성능시험을 거쳐 정식 허가를 신청하였고, 임상적 성능시험계획 승인을 받은 제품이 성
daily-standup.tistory.com
[코로나 검사] 전국 임시 선별 진료소 위치 및 일요일 검사
전국에 위치한 코로나 검사 [임시 검사 진료소]를 업데이트 합니다. 평일과 토요일 운영시간을 확인하시기 바랍니다. 휴일과 주말(일요일)에도 임시 선별소에서는 검사가 가능합니다. 임시 진료
daily-standup.tistory.com
[가락시장] 겨울 과일,채소,수산물 시세를 공개합니다
가락시장은 방어,연어 회 만 먹으러가고 옆에 시장이 뭐하는 곳인지 잘 몰랐었는데 이렇게 많은 과일과 채소들이 거래되고 있는지 몰랐습니다. 가락시장은 완전 새벽에만 거래되
daily-standup.tistory.com
혁신의료기기 지정 현황
연번 품목명 제품 개요 업체명 지정일 1 안과영상검출·진단 보조소프트웨어 인공지능 기술을 적용하여 안저영상의 이상소견을 진단·보조하는 소프트웨어 ㈜뷰노 ’20.7.22. 2 치료용중성자 조사
daily-standup.tistory.com
유럽,미국,한국 탄소중립 프로그램과 에너지 산업
[ 온실가스 배출 현황 ] 현재 온실가스 최다 배출국인 중국의 배출량은 여전히 지속적으로 증가 중이나, 세계 2위 배출국인 미국의 배출량은 점차 감소 추세 독일, 영국, 프랑스, 일본 등 주
daily-standup.tistory.com
중소기업에서 [혁신 제품 지정 제도]와 기업체
[ 우수연구개발 혁신제품 지정 제도 ] 중소벤처기업부 ’혁신제품 지정제도‘는 정부의 기술개발 자금을 지원받아 개발에 성공한 제품 중 기술적 혁신성, 사회적 필요성이 인정된 제품을 혁신
daily-standup.tistory.com



